Claudio De Felice, U.O.C. Terapia Intensiva Neonatale –
Policlinico “S. Maria alle Scotte” Azienda Ospedaliera Universitaria Senese (AOUS) Policlinico “S. Maria alle Scotte” – Siena (Coordinatore del Progetto).
Email c.defelice@ao-siena.toscana.it ; geniente@gmail.com
vi facciamo una breve sintesi di una dei quattro progetti vincitori del bando AIRETT 2021
Una caratteristica chiave della Sindrome di Rett (RTT) è l’alterata regolazione del sistema nervoso autonomo che si manifesta con tachicardia, alterazioni tipiche dell’elettrocardiogramma, salivazione profusa, digrignamento dei denti, anomalie della sudorazione, percezione del dolore e controllo della temperatura corporea e controllo vascolare periferico (Gualniera et al. 2021). La disfunzione autonomica è potenzialmente correlata al rischio aumentato di morte improvvisa. Ricerche precedenti hanno esaminato la variabilità della frequenza cardiaca (heart rate variability, HRV), parametri di ripolarizzazione cardiaca e misure di accoppiamento cardiorespiratorio (Gualniera et al. 2021).
Tuttavia la maggioranza degli studi sull’alterata regolazione del ritmo cardiaco è stata condotta in ambiente ospedaliero e/o senza considerare la fase del sonno. Ad eccezione di pochissimi studi recenti (Rohdin et al. 2007, Carroll et al. 2020, Ramirez et al. 2020, Gualniera et al. 2021, Singh et al. 2022, Suresha et al. 2023), le misure quantitative dei disturbi fisiologici e comportamentali nella RTT sono state prevalentemente affidate a sistemi invasivi e/o eseguibili durante ospedalizzazione (es. polisonnografia, PSG) (Segawa et al. 1992, Marcus et al. 1994, Carotenuto et al. 2012, Amaddeo et al. 2019, Zhang et al. 2022 e Zhang et al. 2022). Il presente progetto multicentrico ha l’obiettivo di esplorare mediante monitoraggio con sistemi affidabili e non invasivi (maglietta “intelligente”) in tempo reale di parametri fisiologici multipli [tracciato ECG e frequenza cardiaca, indice di variabilità della frequenza cardiaca (Heart Rate Variability, HRV), tracciato e dinamica respiratoria e frequenza respiratoria, temperatura cutanea, rilevazione di eventuali urti e caduta, e indice di stress (Stress Factor)] per:
- la ricerca di misure oggettive di gravità utilizzabili nella pratica e ricerca clinica;
- il riconoscimento di caratteristiche fisiologiche specifiche della malattia, potenzialmente correlate con la gravità clinica e tipo di mutazione MECP2;
- l’identificazione di nuovi bersagli potenziali di future terapie nell’ambito del sistema nervoso autonomo.
L’obiettivo primario del presente studio è la validazione della tecnologia indossabile (wearable technology) nella Sindrome di Rett per la valutazione da remoto non-invasiva di funzionalità respiratoria, attività cardiaca e attività motoria durante il ciclo sonno-veglia (24 h). L’identificazione di nuovi potenziali biomarcatori e/o target terapeutici nell’ambito del sistema nervoso autonomo e la misura oggettiva dell’efficacia di un trattamento (misure di outcome) sono fondamentali nel contesto di trial clinici randomizzati. Nel presente studio sarà effettuato un monitoraggio in tempo reale e in ambiente extra-ospedaliero (domicilio)/routine quotidiana dei seguenti parametri fisiologici diretti o derivati:
- tracciato ECG (qualità fino a 4000 Mhz di frequenza di rilevamento) e frequenza cardiaca,
- tracciato e curva dell’atto respiratorio e frequenza respiratoria,
- temperatura cutanea,
- rilevazione urti,
- variabilità della frequenza cardiaca (Heart Rate Variability, HRV),
- “Stress factor”.
Correlazione con diario dei genitori/caregiver rappresentato da risposte 1-5 su scale Likert in schede quotidiane relative alle seguenti categorie:
- energia,
- apparente aspetto sofferenza;
- attenzione-vigilanza;
- irritabilità/agitazione,
- stereotipie delle mani,
- crisi convulsive.
Centri Attualmente Coinvolti
Azienda Ospedaliera Universitaria Senese, Siena; IRCCS Istituto Giannina Gaslini, Genova; ASST Santi Paolo e Carlo, Milano; Azienda Ospedaliera Universitaria G. Martino, Messina.
Disegno: Lo studio multicentrico, della durata complessiva di 24 mesi, è strutturato in 2 Task principali: – Task 1: Confronto wearable technology vs. PSG (IRCSS G. Gaslini, Genova) casistica n=12 pazienti RTT, n=4 per ogni stadio clinico (II-IV); – Task 2. Misura di gravità clinica oggettiva vs. stadio di malattia vs. scale di gravità (Centro Coordinatore AOUS Siena, Azienda Ospedaliera Universitaria, Messina e ASST Santi Paolo e Carlo, Milano) casistica n=24 pazienti RTT, n=8 per ogni stadio clinico (II-IV) vs. n=12 soggetti sani. Popolazione in Studio: n=36 pazienti RTT e n=12 soggetti sani comparabili per età e genere. Criteri di inclusione: – genere femminile; – età >/= 4 anni; – diagnosi clinica con comprovata mutazione patogenetica MECP2; – disponibilità da parte dei genitori/tutore legale della paziente a fornire il proprio consenso libero e informato. Criteri di esclusione: – genere maschile; – pazienti RTT con diagnosi non-in accordo con le linee guida; -assenza di mutazione MECP2 patogenetica; -presenza di mutazioni MECP2 non patogenetiche; – presenza di duplicazione MECP2; – presenza di mutazioni in altri geni patogenetici per sindromi RTT-like (CDKL5, FOXG1).
Dati Preliminari
L’applicabilità di una wearable technology (maglietta intelligente YOUCARE, dispositivo medico indossabile CE, ACCYOURATE Group SpA) nella Sindrome di Rett è attualmente in corso di verifica presso il Centro Coordinatore (AOUS Siena) nell’ambito di uno studio pilota monocentrico (durata 4 mesi) su n=10 pazienti (età media 18,3 anni, range 3,9 – 34,2 anni), approvato dal Comitato Etico CEASVE Regione Toscana (Figura 1). I risultati preliminari dello studio pilota indicano che il monitoraggio continuo domiciliare dei parametri vitali nelle pazienti arruolate è
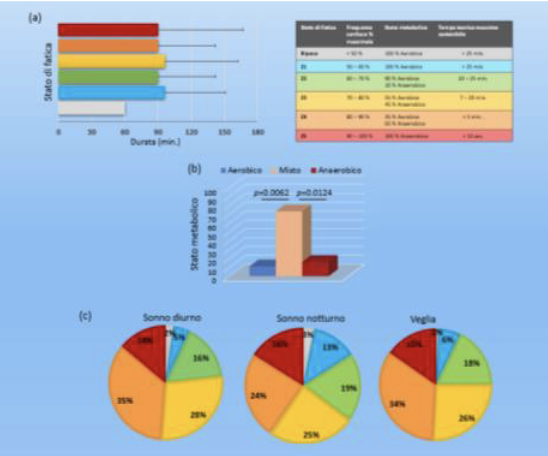
1) fattibile ed accurato, 2) accettato facilmente da pazienti e genitori, 3) confermano la presenza di disfunzione autonomica; e 4) rivelano, per la prima volta, la presenza di uno stato di fatica muscolare cronica finora non noto nella sindrome di Rett (Figura 2).
I dati finali, disponibili entro Luglio 2023, serviranno come dati preliminari e razionale per la richiesta di approvazione, da parte dei Comitati Etici dei centri partecipanti al Progetto multicentrico.
Bibliografia
Gualniera L, Singh J, Fiori F, Santosh P. Emotional Behavioural and Autonomic Dysregulation (EBAD) in Rett Syndrome – EDA and HRV monitoring using wearable sensor technology. J Psychiatr Res. 2021; 138:186-193.
Rohdin M, Fernell E, Eriksson M, Albåge M, Lagercrantz H, Katz-Salamon M. Disturbances in cardiorespiratory function during day and night in Rett syndrome. Pediatr Neurol. 2007; 37:338-44.
Carroll MS, Ramirez JM, Weese-Mayer DE. Diurnal variation in autonomic regulation among patients with genotyped Rett syndrome. J Med Genet 57:786–93; 2020.
Ramirez JM, Karlen-Amarante M, Wang JJ, Bush NE, Carroll MS, Weese-Mayer DE, et al. The pathophysiology of Rett syndrome with a focus on breathing dysfunctions. Physiology. 35:375–90; 2020.
Singh J, Ameenpur S, Ahmed R, Basheer S, Chishti S, Lawrence R, Fiori F, Santosh P. An Observational Study of Heart Rate Variability Using Wearable Sensors Provides a Target for Therapeutic Monitoring of Autonomic Dysregulation in Patients with Rett Syndrome. Biomedicines. 2022; 10:1684.
Suresha PB, O’Leary H, Tarquinio DC, Von Hehn J, Clifford GD. Rett syndrome severity estimation with the BioStamp nPoint using interactions between heart rate variability and body movement. PLoS One. 2023;18:e0266351.
Zhang XY, Spruyt K. A meta-review of standard polysomnography parameters in Rett Syndrome. Front Neurol. 2022; 13:963626.
Zhang X, Smits M, Curfs L, Spruyt K. Sleep Respiratory Disturbances in Girls with Rett Syndrome. Int J Environ Res Public Health. 2022;19:13082.
Segawa M, Nomura Y. Polysomnography in the Rett syndrome. Brain Dev. 1992;14 Suppl:S46-54.
Carotenuto M, Esposito M, D’Aniello A, Rippa CD, Precenzano F, Pascotto A, Bravaccio C, Elia M. Polysomnographic findings in Rett syndrome: a case-control study. Sleep Breath. 2013;17:93-8.
Marcus CL, Carroll JL, McColley SA, Loughlin GM, Curtis S, Pyzik P, Naidu S. Polysomnographic characteristics of patients with Rett syndrome. J Pediatr. 1994;125:218-24.
Amaddeo A, De Sanctis L, Arroyo JO, Khirani S, Bahi-Buisson N, Fauroux B. Polysomnographic findings in Rett syndrome. Eur J Paediatr Neurol. 2019;23:214-221.
FiFigura 1. Disegno dello studio pilota
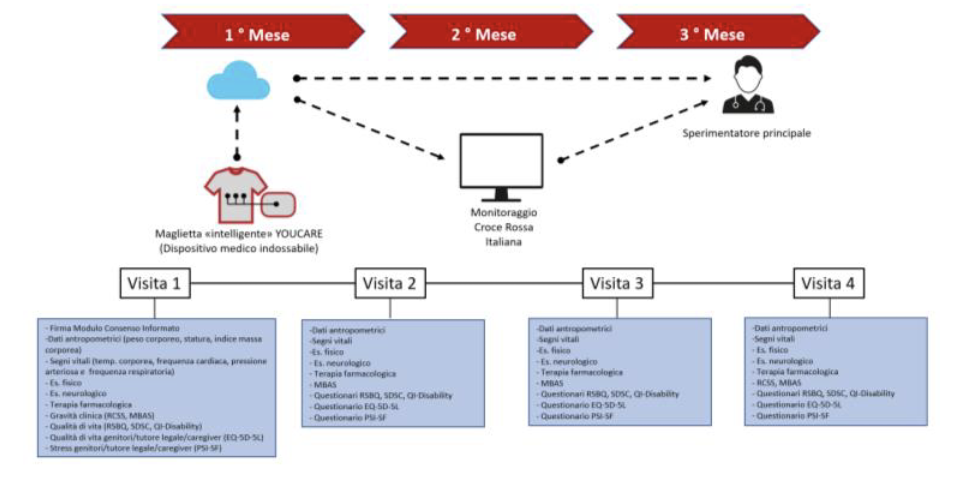
Figura 2. Stato di fatica nella sindrome di Rett: durata (a), stato metabolico (b), e in funzione del ciclo sonno-veglia e sonno diurno (c)