Sintesi della pubblicazione: C. De Felice, M. Rossi, S. Leoncini, G. Chisci, C. Signorini, G. Lonetti, L. Vannuccini, D. Spina,A. Ginori, I. Iacona, A. Cortelazzo, A. Pecorelli, G. Valacchi, L.Ciccoli, T. Pizzorusso, J. Hayek. Inflammatory Lung Disease in Rett Syndrome. Mediators of Inflammation In Press (Volume 2014, Article ID 560120,15 pages http://dx.doi.org/10.1155/2014/560120).
Claudio De Felice,1 Marcello Rossi,2 Silvia Leoncini,3,4 Glauco Chisci,5 Cinzia Signorini,3 Giuseppina Lonetti,6 Laura Vannuccini,2 Donatella Spina,7 Alessandro Ginori,7 Ingrid Iacona,2 Alessio Cortelazzo,4,8 Alessandra Pecorelli,3,4 Giuseppe Valacchi,9 Lucia Ciccoli,3 Tommaso Pizzorusso,6,10 and Joussef Hayek4
1 Terapia Intensiva Neonatale, Azienda Ospedaliera Universitaria Senese (AOUS), Viale M. Bracci 16,53100 Siena, Italy
2 Fisiopatologia Respiratoria e Riabilitazione, AOUS, Viale M. Bracci 16, 53100Siena,
3 Dipartimento di Medicina Molecolare e dello Sviluppo, Università di Siena, Via A. Moro 2, 53100 Siena
4 Neuropsichiatria Infantile, AOUS, Viale M. Bracci 16, 53100 Siena
5 Dipartimento di Chirurgia Maxillo-Facciale, Università di Siena,Viale M. Bracci 16, 53100 Siena
6 Istituto di Neuroscienze, CNR, Via G. Moruzzi 1, 56124 Pisa
7 Anatomia Patologica, AOUS, Viale M. Bracci 16, 53100 Siena
8 Dipartimento di Biotecnologie Mediche, Università di Siena, Via A. Moro 2, 53100 Siena
9 Dipartimento di Scienze della Vita e Biotecnologia, Università di Ferrara, Via Borsari 46, 44100 Ferrara, Italy
10 Dipartimento di Neuroscienze, Psicologia, Ricerca Farmaci e Salute Pediatrica (Neurofarba), Università di Firenze, Area S. Salvi Pad. 26, 50135 Firenze
La disfunzione respiratoria sta assumendo un ruolo sempre più centrale nella patologia multi-sistemica della sindrome di Rett (RTT). Il nostro gruppo di studio multidisciplinare si interessa da alcuni anni della patologia respiratoria nelle pazienti RTT affrontando il tema da una prospettiva in un certo senso rovesciata del problema. Finora gli studi dei vari gruppi internazionali sono stati focalizzati sul disturbo neuro-autonomico del respiro e sulla immaturità del tronco encefalico come causa principale delle multiformi irregolarità respiratorie nella RTT [Julu et al. 2008, Gallego 2012]. Le apnee che si riscontrano frequentemente nelle pazienti sono state finora attribuite a fenomeni essenzialmente “centrali”. Dai nostri studi emerge un quadro notevolmente differente. La nostra scoperta nel 2009 dello stress ossidativo (SO) sistemico e dell’ipossia subclinica nella sindrome di Rett classica ci ha portato a studiare il ruolo degli scambi respiratori polmonari [De Felice et al. 2009]. Nello stesso anno abbiamo identificato in maniera indiretta le anomalie degli scambi respiratori polmonari (gas exchange abnormality, GEA) utilizzando un prototipo brevettato dal Dott. Marcello Rossi e dall’Ing. Laura Vannuccini che permette di misurare anche in pazienti “non cooperanti” gli scambi respiratori in modo rapido, accurato e riproducibile . Un’indagine TAC ad alta risoluzione del polmone ci aveva fatto descrivere nel 2010 in oltre metà delle pazienti esaminate un quadro radiologico polmonare sorprendentemente simile a quello della bronchiolite respiratoria con malattia interstiziale (Respiratory Bronchiolitis-Associated Interstitial Lung Disease, RB-ILD), una patologia infiammatoria polmonare relativamente rara che è associata al fumo di sigaretta nel 95% dei casi [De Felice et al. 2010].
Nella presente ricerca abbiamo esaminato le relazioni fra la presenza di apnee/ipopnee, l’anomalia degli scambi respiratori e l’equilibrio pro-ossidanti/anti-ossidanti in un numero ampio di pazienti RTT con la forma classica della malattia (n=228; età media 12,9 ± 7,9 anni, range: 1,5-32) (Tabella 1). L’analisi degli scambi gassosi polmonari indica che solo 19,3% (44/228) pazienti RTT presenta un pattern di scambio normale. Circa 28% delle pazienti RTT presenta un pattern definito “low” (Figura 1 A) in cui è presente perfusione in aree polmonari scarsamente ventilate, mentre 32% presenta un pattern “high” che indica la presenza di aree polmonari abbondantemente ventilate ma scarsamente perfuse (Figura 1 B). Quasi 16% (36/228) delle pazienti RTT presenta un pattern misto (Figura 1 C) e il rimanente 4,8% presenta un pattern di “simple mismatch” (Figura 1 D).
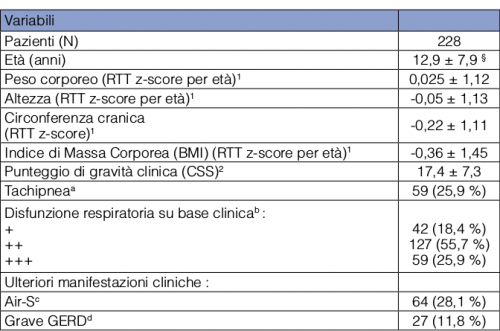
1 Gli z-score (procedimento di standardizzazione della curva gaussiana di distribuzione dei dati in cui il valore zero corrisponde alla media dei valori con la normalità compresa all’interno dell’intervallo ± 2) per età sono riferiti alle tabelle di crescita specifiche per la sindrome di Rett [Tarquinio DC et al. 2012]. 2 Il punteggio di gravità clinico era calcolato in accordo a Neul et al. [Neul JL et al. 2008]. a La tachipnea era definita come frequenza respiratoria > 1,8 volte rispetto a quella attesa per età e sesso; b La disfunzione respiratoria era classificata sulla base della scala di gravità clinica di Percy [Colvin L et al. 2003]; § media ± SD; c Air-S: disfagia; d GERD: reflusso gastro-esofageo.
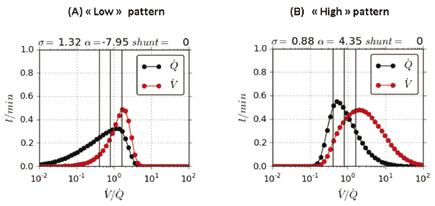 Figura 1. Anomalie rappresentative dello scambio gassoso polmonare in pazienti con sindrome di Rett e mutazione MECP2.
Figura 1. Anomalie rappresentative dello scambio gassoso polmonare in pazienti con sindrome di Rett e mutazione MECP2.
Un’analisi accurata dei vari parametri respiratori in funzione del tipo di anomalia degli scambi gassosi polmonari (GEA) indica che l’iperventilazione è più evidente nei pazienti con pattern “high”, che l’ipossia è più evidente nei pazienti con pattern “low” o misto e che non ci sono differenze significative in termini di accumulo di CO2 tra i vari pattern. Un punto interessante è che l’iperventilazione (probabilmente compensatoria piuttosto che conseguenza di un’immaturità dei centri respiratori encefalici) si associa ad un aumento dello spazio morto fisiologico di Bohr. In altri termini, l’aumentata aria alveolare non riesce a partecipare agli scambi gassosi alveolo-arteriosi (Tabella 2).
relazioni tra modelli di alterazioni del rapporto ventilazione-perfusione polmonare (V/Q) e variabili respiratorie.
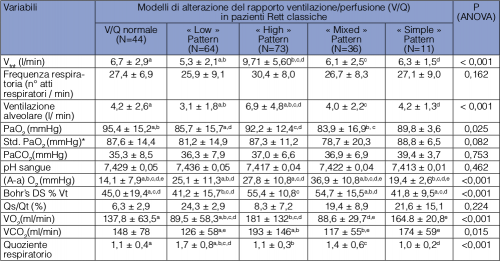 I dati sono espressi come medie ± SD. I caratteri in grassetto indicano le differenze statisticamente significative. Vtot: ventilazione totale; Bohr’s DS: spazio morto fisiologico, calcolato mediante l’equazione di Bohr che, quantificando il rapport tra spazio morto fisiologico e volume tidal totale (Vd/Vt=PaCO2-PeCO2/PaCO2), fornisce informazioni quantitative sulla quota ventilatoria non utilizzabile ai fini degli scambi respiratori; (A-a) O2, O2 gradiente alveolo–arterioso; Vt, volume tidal; Qs/Qt, shunt funzionale polmonare; VO2, uptake dell’ossigeno; VCO2, produzione di CO2;* valori calcolati secondo la formula di Sorbini et al. che tiene conto del fattore ipocapnia: PaO2 standard = 1.66 x PaCO2 + PaO2 – 66.4 [Sorbini CA et al. 1968]; Quoziente respiratorio= VCO2/VO2.
I dati sono espressi come medie ± SD. I caratteri in grassetto indicano le differenze statisticamente significative. Vtot: ventilazione totale; Bohr’s DS: spazio morto fisiologico, calcolato mediante l’equazione di Bohr che, quantificando il rapport tra spazio morto fisiologico e volume tidal totale (Vd/Vt=PaCO2-PeCO2/PaCO2), fornisce informazioni quantitative sulla quota ventilatoria non utilizzabile ai fini degli scambi respiratori; (A-a) O2, O2 gradiente alveolo–arterioso; Vt, volume tidal; Qs/Qt, shunt funzionale polmonare; VO2, uptake dell’ossigeno; VCO2, produzione di CO2;* valori calcolati secondo la formula di Sorbini et al. che tiene conto del fattore ipocapnia: PaO2 standard = 1.66 x PaCO2 + PaO2 – 66.4 [Sorbini CA et al. 1968]; Quoziente respiratorio= VCO2/VO2.
L’analisi poligrafica, pur confermando l’elevata frequenza di apnee / ipopnee durante lo stato di veglia o di sonno nella Rett, dimostra la netta predominanza degli eventi di tipo ostruttivo (= quando si verifica un blocco meccanico al flusso d’aria) su quelli di origine centrale (= quando i centri encefalici deputati al controllo della respirazione “si dimenticano” di respirare) (Tabella 3).
Tabella 3. Monitoraggio cardiorespiratorio in pazienti con sindrome di Rett in forma classica (n=228).
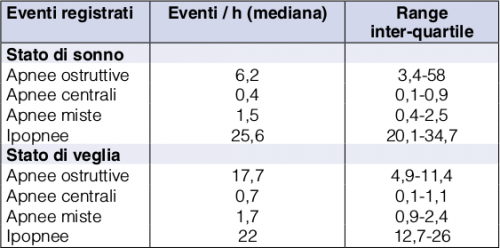
Le apnee sono definite come una diminuzione del flusso ventilatorio > 90% per un periodo di tempo ≥10 sec. Le ipopnee sono definite come una diminuzione del flusso ventilatorio > 50% per un periodo di tempo ≥10 sec associata a una diminuzione della saturazione di ossigeno ≥3% [West JB 1969]. Le apnee ostruttive sono definite come interruzione del flusso ventilatorio per un periodo di tempo ≥10 sec associata a un persistente sforzo respiratorio da parte del diaframma e degli altri muscoli respiratori, mentre le apnee centrali sono definite come una interruzione del flusso ventilatorio per un periodo di tempo ≥10 sec in assenza di sforzo respiratorio associato. Le apnee miste sono definite come eventi respiratori che iniziano come apnee centrali e terminano come apnee ostruttive.
Questo dato è sorprendentemente parallelo ad un reperto sperimentale del 2010 osservato da parte di un gruppo di ricerca francese [Voituron et al. 2010].
L’analisi della relazione tra modelli di ventilazione/perfusione polmonare (V/Q) e stato redox/antiossidanti indica che lo SO è praticamente assente nel gruppo di pazienti RTT classica con normali scambi gassosi polmonari, mentre una significativa anomalia redox è presente nei pazienti con gli altri pattern sebbene con differenze inter-gruppo (Tabella 4).
Tabella 4. Relazione tra modelli di ventilazione / perfusione polmonare (V/Q) e stato redox / antiossidante in pazienti con RTT classica (n=228).
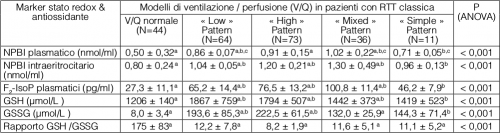 I dati sono espressi come medie ± SD. I caratteri in grassetto indicano differenze statisticamente significative; le lettere in apice indicano differenze post-hoc statisticamente significative. Legenda:NPBI: ferro libero non complessato a proteine (non protein bound iron);?F2-IsoP: F2-isoprostani; GSH: glutatione ridotto; GSSG: glutatione ossidato.
I dati sono espressi come medie ± SD. I caratteri in grassetto indicano differenze statisticamente significative; le lettere in apice indicano differenze post-hoc statisticamente significative. Legenda:NPBI: ferro libero non complessato a proteine (non protein bound iron);?F2-IsoP: F2-isoprostani; GSH: glutatione ridotto; GSSG: glutatione ossidato.
I modelli murini sperimentali hanno prodotto un enorme balzo in avanti delle conoscenze sui meccanismi molecolari nella RTT, ma bisogna ricordare che i modelli sono appunto tali: cercano di riassumere le principali caratteristiche della malattia umana ma sappiamo bene che la RTT del topo non è necessariamente equivalente alla RTT delle bimbe. Un ottimo esempio di questo limite è la dimostrazione della differenza del fenotipo respiratorio in funzione del tipo di mutazione Mecp2 in differenti modelli murini. [Bissonnette et al. 2014]. Tuttavia il topo Mecp2 nullo è considerato da tempo un modello molto utile per comprendere i meccanismi del deficit funzionale di MeCP2 nelle bambine affette. In questo studio abbiamo quindi aggiunto un esame istologico del polmone in esemplari di un modello di topo Mecp2 nullo [Chen et al. 2001] forniti dal laboratorio del prof. Tommaso Pizzorusso e confrontati con i corrispettivi controlli sani (wild type, wt).
I risultati istologici indicano la presenza di una bronchiolite linfocitaria aspecifica e un’alveolite desquamativa nei polmoni dei topi Mecp2 nulli (Figura 2).
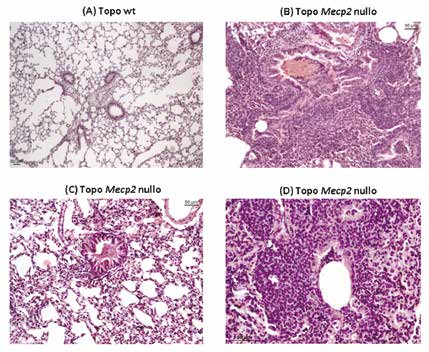 Figura 2. Quadro istologico di bronchiolite linfocitaria aspecifica e alveolite desqua- mativa nei polmoni dei topi Mecp2 nulli. (A) Topo wild-type (ingrandimento 25x), (B) Topo Mecp2 nullo (ingrandimento 50x), (C) Topo Mecp2 nullo (ingrandimento 50x), (D) Topo Mecp2 nullo (ingrandimento 200x).
Figura 2. Quadro istologico di bronchiolite linfocitaria aspecifica e alveolite desqua- mativa nei polmoni dei topi Mecp2 nulli. (A) Topo wild-type (ingrandimento 25x), (B) Topo Mecp2 nullo (ingrandimento 50x), (C) Topo Mecp2 nullo (ingrandimento 50x), (D) Topo Mecp2 nullo (ingrandimento 200x).
Conclusioni
Il nostro studio conferma il concetto che non esista un unico meccanismo alla base della complessa disfunzione respiratoria nella RTT in cui probabilmente giocano molti attori co-protagonisti fra i quali abbiamo identificato, oltre alle ostruzioni delle alte vie respiratorie su base meccanica sia durante lo stato di veglia che durante il sonno, l’anomalia degli scambi respiratori polmonari che sembra la vera chiave del fenotipo respiratorio delle bimbe RTT e della presenza di SO perlomeno nella forma classica della malattia. Inoltre, i bronchioli respiratori sembrano essere – nella malattia umana come in almeno un modello sperimentale – un target infiammatorio finora non riconosciuto.
Referenze bibliografiche:
- P. O. Julu, I.W. Engerstr¨om, S.Hansen et al., “Cardiorespiratory challenges in Rett’s syndrome,”TheLancet, vol. 371, no. 9629, pp. 1981–1983, 2008.
- J. Gallego, “Genetic diseases: congenital central hypoventilation, Rett, and Prader-Willi syndromes,” Comprehensive Physiology,vol. 2, no. 3, pp. 2255–2279, 2012.
- C. De Felice, L. Ciccoli, S. Leoncini et al., “Systemic oxidative stress in classic Rett syndrome,” Free Radical Biology and Medicine, vol. 47, no. 4, pp. 440–448, 2009.
- C. De Felice, G. Guazzi, M. Rossi et al., “Unrecognized lung disease in classic Rett syndrome: a physiologic and high resolution CT imaging study,” Chest, vol. 138, no. 2, pp. 386–392, 2010.
- J. L. Neul, P. Fang, J. Barrish et al., “Specific mutations in Methyl-CpG-Binding Protein 2 confer different severity in Rett syndrome,” Neurology, vol. 70, no. 16, pp. 1313–1321, 2008.
- L.Colvin, S. Fyfe, S. Leonard et al., “Describing the phenotype in Rett syndrome using a population database,” Archives of Disease in Childhood, vol. 88, no. 1, pp. 38–43, 2003.
- D. C. Tarquinio, K. J. Motil, W. Hou et al., “Growth failure and outcome in Rett syndrome: specific growth references,” Neurology, vol. 79, no. 16, pp. 1653–1661, 2012
- C. A. Sorbini, V. Grassi, E. Solinas, and G. Muiesan, “Arterial oxygen tension in relation to age in healthy subjects,” Respiration, vol. 25, no. 1, pp. 3–13, 1968.
- N. Voituron, C. Menuet, M. Dutschmann, and G. Hilaire, “Physiological definition of upper airway obstructions inmouse model for Rett syndrome,” Respiratory Physiology & Neurobiology, vol. 173, no. 2, pp. 146–156, 2010.
- Bissonnette JM, Schaevitz LR, Knopp SJ, Zhou Z. Respiratory phenotypes are distinctly affected in mice with common Rett syndrome mutations MeCP2 T158A and R168X. Neuroscience. 2014 Mar 10;267C:166-176.
- R Z. Chen, S. Akbarian, M. Tudor, and R. Jaenisch, “Deficiency of methyl-CpG binding protein-2 in CNS neurons results in a Rett-like phenotype in mice,” Nature Genetics, vol. 27, no. 3, pp. 327–331, 2001.

